国内外研究现状
该研究的理论支持可分为三部分:载药胶束,载体平台可注射凝胶,以下将分别介绍这三方面的国内外研究现状。
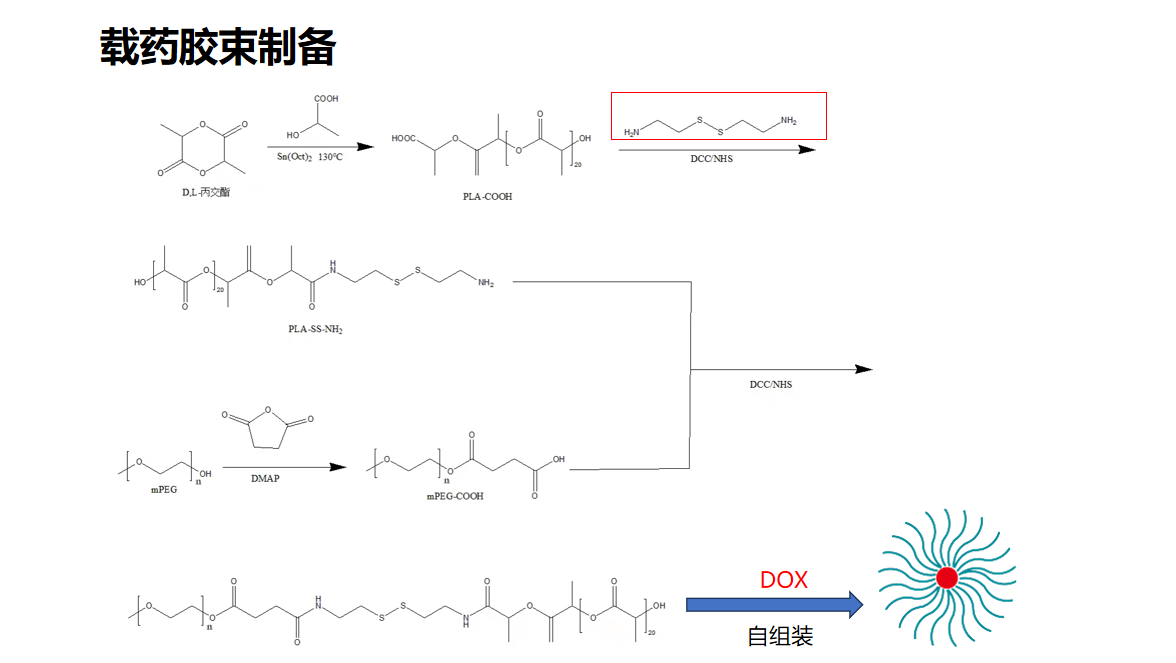
1.载药胶束
载药胶束作为一种重要的纳米药物载体,在国内外的研究和应用中有着广泛的关注。以下是一些关键的研究现状:
(1)ROS响应型核交联聚合物胶束的制备与研究:研究团队针对肿瘤微环境中活性氧簇(ROS)水平高于正常细胞的特点,设计并合成了基于硫缩酮键的ROS响应型两亲性载体材料mPEG-b-PTK。通过光交联法,这些材料能够自组装形成核交联胶束,有效包裹抗癌药物阿霉素(DOX),并展现出良好的生物相容性和稳定性。在ROS存在的情况下,硫缩酮键能够迅速断裂,导致胶束结构解体并释放药物,从而在肿瘤部位实现精准的药物递送。实验结果表明,这种核交联载药胶束在HeLa细胞中具有出色的内化能力,对正常细胞的毒性较低,而对癌细胞的毒性较高,显示出良好的抗癌活性。此外,该载药系统还能实现疏水性小分子药物和亲水性大分子药物的分区共载,有望实现两种不同药物的协同治疗作用。尽管如此,该载药系统的生物降解性和体内抗肿瘤效果仍需进一步研究,以验证其在临床应用中的潜力。[3]
(2)自组装NIPAM-PEG-NIPAM聚合物纳米胶束:聚合物胶束包括自聚集胶束、单分子胶束和交联的胶束,可采用化学结合法、物理包载和聚离子复合法包载药物。药物分子在聚合物胶束中的分布以及聚合物的降解行为决定了药物的释放速率。如Marjan Bagheri?Meyabad团队用于递送锌原卟啉的自组装NIPAM-PEG-NIPAM聚合物纳米胶束。由于血红素加氧酶抑制剂锌原卟啉(ZnPP)溶解性差,不良反应多,其开发了基于PNIPAM-PEG-PNIPAM三嵌段共聚物的热响应聚合物胶束,用于将ZnPP递送到前列腺癌细胞(PC3)。热敏性赋予纳米载体更多的结构稳定性和更少的药物泄漏。聚合物表征之后,平均临界胶束浓度(CMC)和最低临界溶液温度(LCST)分别为22.32 μg/mL和36.20 °C。制备的载药胶束在37 °C下的平均直径为148 nm,包埋效率为98%,载药量为35%。根据体外结果,纳米胶束的ZnPP释放速率遵循温度依赖性方式。通过对负载ZnPP的胶束处理的PC3细胞进行 MTT 测定获得的IC50比游离药物低36%(P<0.01),这表明其制备制剂的毒性有所改善。与游离药物相比,在相同的ZnPP浓度下,载药胶束表现出显着更强的诱导PC3细胞凋亡的能力。此外,流式细胞术和共聚焦显微镜评估证实了其制备的纳米颗粒的细胞摄取。[4]
(3)响应型纳米载药胶束的制备和性质研究:研究者基于过氧化氢等刺激响应性的两亲性聚合物,能够自组装成球形胶束并包载疏水性药物,具备载药量高、响应灵敏度高、选择性好的优势。如张川团队在研究中设计合成了具有响应性和降解性的光化学治疗肿瘤的纳米载药体系。通过开环聚合、高温缩聚以及化学修饰等方法,制备了一种可降解的谷胱甘肽敏感性混合载药胶束DCBM。其次,为了进一步提升光化疗的效果,引入一氧化氮(NO)以增强协同热化疗的效果,解决化疗中的耐药问题。再次,结合亚细胞层面的光动力治疗和细胞层面的化疗提升光化疗的效果。通过简单化学键连的方式,合成了一种过氧化氢敏感性、具有线粒体靶向能力的混合胶束,赋予其化疗和光动力治疗的能力。最后,尝试将阳离子纳米微球作为药物载体应用到癌症的光化疗之中,拓展阳离子型聚合物微球的应用范围。以三甲基乙烯苄基氯化铵和丙烯酸为
单体,通过乳液聚合的方法合成了一种pH响应性阳离子纳米微球 VANPs,并通过VANPs与药物小分子之间的库仑力作用,设计制备了一种pH响应性、阳离子型的纳米药物载体ID@VANPs。[5]
(4)新型的氧化还原双重响应型前药纳米载药胶束:通过将疏水性药物紫杉醇(PTX)与油酸(OA)结合,这些前药结合物在水溶液中自组装成胶束结构,用于提高癌症化疗药物紫杉醇(PTX)的疗效。研究者设计了两种不同的PTX-油酸结合物,一种包含硫醚键(PTX-S-OA),另一种插入了二硫醚(PTX-2S-OA),以利用肿瘤内部的氧化还原特性进行药物释放。结果表明,PTX-S-OA比PTX-2S-OA对氧化还原刺激更敏感,能够更快速且选择性地释放出PTX。PEG修饰的PTX-S-OA纳米组装体具有高达57.4%的药物载量,在体内实验中显示出显著的抗肿瘤活性。由于其氧化还原双重响应特性,这些纳米胶束能够在肿瘤微环境的特定刺激下快速释放药物,从而提高了药物的靶向性和治疗效果。[6]
2.载体平台
(1)靶向聚合物纳米载体在黑色素瘤治疗中的应用:在本研究中,研究人员开发了一种具有靶向性和免疫激活能力的聚合物纳米载体平台,用于黑色素瘤的免疫治疗。这种纳米载体通过特定的靶向配体cRGD和mannose修饰,能够精确识别并结合到肿瘤细胞上,提高肿瘤特异性摄取。它能够直接诱导黑色素瘤细胞发生免疫原性细胞死亡(ICD),释放损伤相关分子模式(DAMPs),从而增强垂死癌细胞的抗原性,促进树突状细胞的募集和成熟,改善抗原呈递。纳米载体展现出稳定的物理化学特性,包括均匀的粒径、稳定的zeta电位和类球形的外貌,这些特性有助于其在体内的稳定性和生物分布。此外,纳米载体通过网格蛋白介导的内吞作用进入肿瘤细胞,唾液酸介导的受体靶向作用显著增加了肿瘤细胞对纳米载体的摄取。实时定量PCR和Western Blot法检测结果证实了纳米载体/siMUC1具有较好的基因沉默效率和调控蛋白表达水平的能力,有效下调胆固醇合成,减少耐药相关膜泵蛋白的表达,改善肿瘤周围的炎性微环境。在体内外实验中,纳米载体/siMUC1展现出显著的抑瘤和抑制肿瘤转移的能力,为黑色素瘤的综合治疗提供了新的策略和理论依据。[7]
(2)pH响应SPPI基因载体:研究团队着眼于肾癌治疗中普遍存在的舒尼替尼耐药性问题,开发了一种新型的靶向E-selectin受体的自组装纳米基因载体SPPI。该载体基于聚乙二醇亚胺(PEI)构建,并通过修饰聚乙二醇(PEG)和布洛芬(IBU),在PEG一端键接唾液酸(SA),成功合成了SA-PEG-PEI-IBU(SPPI)。SPPI的设计旨在通过递送小干扰RNA(siRNA)来沉默MUC1的表达,从而调控肾癌细胞的脂质代谢,逆转对舒尼替尼的耐药性。实验结果表明,SPPI胶束具有良好的基因装载能力,稳定的粒径和zeta电位,以及类球形的外貌,这些特性使得SPPI能够有效地进入细胞内部,显著下调胆固醇含量,并发挥预期的耐药调控作用。通过共聚焦显微镜和流式细胞仪的实验,研究团队发现SPPI载体主要通过网格蛋白的介导作用进入肿瘤细胞,且唾液酸介导的受体靶向作用显著增加了肿瘤细胞对SPPI载体的摄取。此外,实时定量PCR和Western Blot法检测结果显示,SPPI/siMUC1展现出较好的基因沉默效率和调控蛋白表达水平的能力,细胞的脂质代谢物质胆固醇的合成也明显减少,由此导致的耐药相关的膜泵蛋白P-GP,ABCG2,MRP1的表达量随之下调,有效改善了肿瘤组织周围的炎性微环境。在体内实验中,SPPI/siMUC1载药体系展现出明显的抑瘤及抑制肿瘤转移的能力,表明该载体系统在体内外均能有效抑制肿瘤生长和转移,为肾癌的综合治疗提供了新的策略和理论依据。[8]
(3)温度敏感性多肽/介孔二氧化硅(MSN)纳米药物载体:通过将温敏亮氨酸拉链型多肽(Pep)接枝到MSN表面,并利用二硫键进行连接,以实现药物的控释。这种载体能够响应肿瘤区域的高温环境和高浓度谷胱甘肽(GSH),从而促进抗癌药物阿霉素(DOX)的释放。[9]
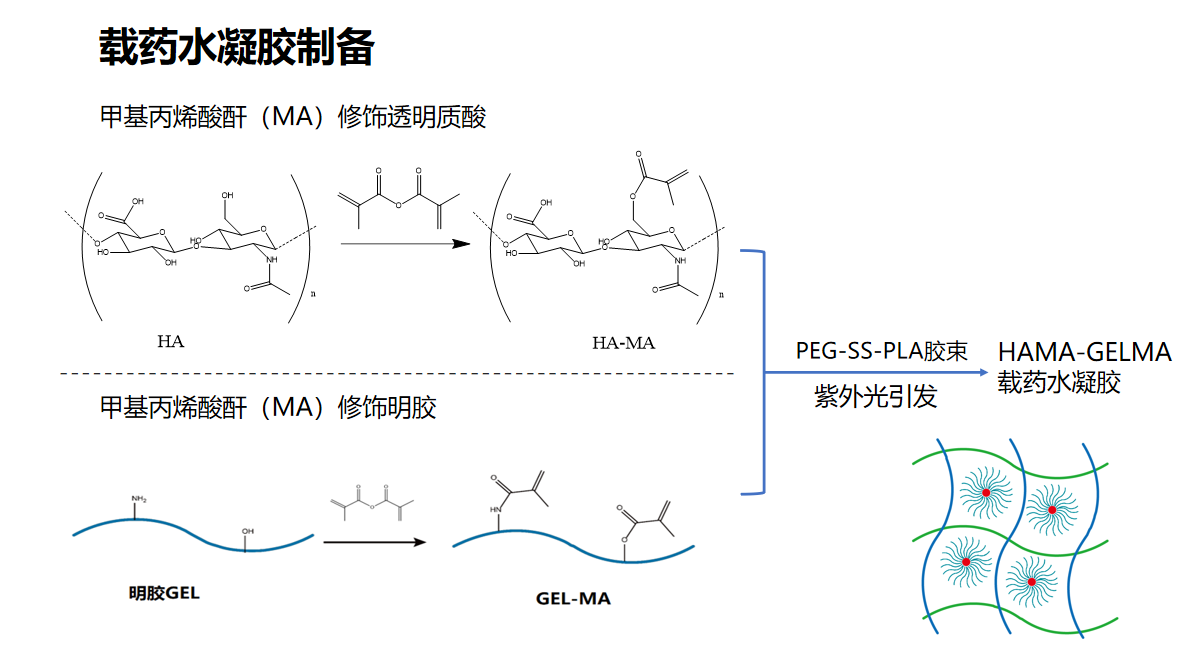
3.可注射凝胶
(1)pH敏感性可注射水凝胶的制备和性能:研究团队研究了一种基于壳聚糖、聚乙二醇和肝素的pH响应性可注射水凝胶的制备和性能,该水凝胶通过席夫碱反应形成,并用于负载具有抗肝纤维化活性的PIGF-2123-144-BiPPB-mimIFNγ融合蛋白。研究中,通过1H-NMR和FT-IR等技术成功表征了NSCS、DF-PEG-DF和Hep-ADH三种目标聚合物,并通过优化醛基和氨基的摩尔比,制备了稳定性好的水凝胶,其中醛基和氨基的最佳比例为0.45。所得水凝胶在40-60秒内成胶,具有良好的可注射性和自愈合能力,这些特性通过试管倒置法、体外注射实验和宏观自愈实验得到验证。扫描电镜(SEM)和流变仪测试表明,水凝胶具有疏松多孔结构和优异的机械性能。体外降解实验显示,水凝胶在pH 6.0的缓冲液中降解速度显著快于pH 7.4的缓冲液,表明其显著的pH响应性。细胞相容性实验通过CCK-8法和Calcein-AM染色法表明,水凝胶对肝细胞和HSC细胞具有良好的生物相容性。最后,通过将水凝胶注射到小鼠皮下,观察到水凝胶在体内具有良好的生物降解性能。这些结果表明,所制备的水凝胶作为一种新型的药物递送系统,在肝纤维化治疗中具有显著的应用潜力。[10]
(2)pH敏感型双载药水凝胶在食管癌治疗中的应用:研究团队成功开发了一种pH响应型、可注射的双载药水凝胶药物递送系统(CS-BA-PVA@Cu/CDDP),用于食管鳞状细胞癌(ESCC)的治疗。该水凝胶由壳聚糖、聚乙烯醇和3-羧基苯硼酸构成,通过硼酸酯键交联形成三维网络结构,共载Cu2+和CDDP,展现出良好的生物相容性和生物可降解性。在弱酸性肿瘤微环境中,水凝胶能够响应性地释放药物,增加肿瘤组织中的药物蓄积,并通过类芬顿反应产生羟基自由基,消耗GSH,增强CDDP的化疗效果,降低肿瘤细胞对CDDP的耐药性。体外细胞实验和体内动物实验均证实了其显著的抗肿瘤效果,包括抑制ESCC细胞的增殖、迁移,并诱导细胞凋亡。机制研究揭示,CS-BA-PVA@Cu/CDDP能诱导ESCC细胞发生铜死亡,并通过内质网应激诱导免疫原性细胞死亡,促进树突状细胞成熟,激活抗肿瘤免疫反应,抑制远处肺转移瘤的发生,为ESCC的安全和有效治疗提供了新的思路。[11]
(3)可注射荧光硫化铋/金纳米簇水凝胶:以生物相容性良好的壳聚糖(CS)和硫化铋-金纳米簇纳米颗粒(Bi2S3-Au NCs NPs)为原料,制备了具有肿瘤术后残余组织光热治疗和促进术后伤口愈合功能的新型水凝胶敷料。通过在CS上接枝具有贻贝类活性的邻苯二酚基团,提高了水凝胶与组织的黏附性。在室温(25℃)下,邻苯二酚改性壳聚糖(CHI-C)和Bi2S3-Au NCs NPs经过简单搅拌混匀后,即可形成交联网络。制备的Bi2S3-Au NCs-CHI-C水凝胶可在1 min内在小鼠黑色素瘤术后伤口原位形成交联网络,并且在808 nm近红外光照射下,其温度可升至49.2 ℃,从而可有效杀死残余肿瘤细胞。在365 nm紫外光照射下,此水凝胶发射强烈的红色荧光,可用于实时精准监测其伤口填充情况,有利于伤口特别是不规则伤口的愈合。[12]
参考文献出处:
[1]周小果,郭娜,段秋立,等.血清MMP-9,ProGRP及内皮素的水平与非小细胞肺癌分期的相关性分析[J].实用癌症杂志, 2024, 39(9):1443-1445.
[2]Alrehaili A A , Gharib A F , Karam R A ,et al.Clinical significance of plasma MMP‐2 and MMP‐9 levels as biomarkers for tumor expression in breast cancer patients in Egypt[J].Molecular Biology Reports, 2020, 47(2):1153-1160.
[3]李蒲.ROS响应型核交联聚合物胶束载药系统的构建及抗肿瘤研究[D].成都大学,2024.
[4]Marjan M B ,Hamidreza M ,Parisa N , et al.Self-assembled NIPAM–PEG–NIPAM polymeric nanomicelles for the delivery of zinc protoporphyrin: a potential stimuli-triggered cancer treatment approach[J].Journal of Materials Science,2024,59(7):3049-3065.
[5]张川.多重响应性纳米载药体系构筑及在肿瘤光化疗方面的应用[D].吉林大学,2019.
[6]Luo C , Sun J , Liu D ,et al.Self-Assembled Redox Dual-Responsive Prodrug-Nanosystem Formed by Single Thioether-Bridged Paclitaxel-Fatty Acid Conjugate for Cancer Chemotherapy[J].Nano Letters, 2016:5401.DOI:10.1021/acs.nanolett.6b01632.
[7]Guo Y , Li Y , Zhang M ,et al.Polymeric nanocarrier via metabolism regulation mediates immunogenic cell death with spatiotemporal orchestration for cancer immunotherapy[J].Nature Communications, 15(1):1-20[2024-11-10].
[8]曾现虎.调控脂质代谢影响肾癌耐药性的靶向基因载体构建及其生物评价[D].青岛大学,2023.
[9]徐俊、刘洪来、徐首红.温度敏感性多肽/介孔二氧化硅纳米药物载体的制备[C]//中国化学会第十七届全国胶体与界面化学学术会议.2019.
[10]莫春香.pH响应性可注射水凝胶的制备、性能及其负载胶原高亲性蛋白的研究[D].南华大学,2022.
[11]张炎晖.pH响应型双载药可注射水凝胶在食管鳞状细胞癌治疗中的应用及机制研究[D].中国人民解放军海军军医大学,2024.
[12]李卓,杨绍贤,刘蕊,等.可注射荧光硫化铋/金纳米簇水凝胶用于肿瘤术后光热治疗和促进伤口愈合性能分析[J].分析化学,2024,52(07)
 大学生创新创业训练计划管理系统
大学生创新创业训练计划管理系统